Вода и ее применение в современных технологияхСтраница 9
Этот поразительный и малопонятный результат эксперимента имеет место не только в лабораторных условиях, но и в природе. При повышении давления водяной газ (пар) не образует тумана и остается прозрачным, а при разрежении туман образуется. Правда, последнее происходит при наличии центров конденсации (пылинок), но их в атмосфере всегда достаточно.
Помимо описанных аномалий у этого удивительного вещества, каким является вода, существуют и другие аномалии (например, аномальная дисперсия, рассеяние, в области электрических и световых лучей и др.), но на них, чтобы не утруждать читателя, мы останавливаться не будем.
1.7 Испарение, транспирация, сублимация и конденсация.
Общеизвестно, что испарение—переход вещества из жидкого или твердого состояния в газообразное (в пар). Обычно под испарением жидкости понимают превращение ее в пар, а испарение твердых тел называется сублимацией (или возгонкой). Обратный процесс, т. е. переход вещества из газообразного состояния в жидкое, именуется конденсацией. Испарение воды с поверхности растений носит название транспирации.
При испарении молекулы переходят из жидкости в пар, преодолевая силы молекулярного сцепления в жидкости. Процесс испарения протекает изотермически, т. е. при постоянной температуре. Скорость испарения определяется массой жидкости, испаряющейся за единицу времени с единицы поверхности. Одной из количественных характеристик процесса испарения воды в атмосферу является дефицит влажности, определяемый разностью между предельной упругостью водяного пара для данной температуры и фактической упругостью.
Если воздух в помещении полностью насыщен парами воды или если из наполненного до краев стакана вода не убывает, но и не прибывает, это значит, что испарение отсутствует, т. е. мы имеем состояние динамического равновесия.
До последнего времени считалось, что лед может переходить в пар, минуя жидкую фазу, т. е. Происходит процесс сублимации. Однако последние более детальные исследования показали, что это далеко не так. В действительности поверхность льда покрыта даже при отрицательных температурах переохлажденной квазижидкой пленкой связанной воды. Таким образом, испаряется не лед, а непрерывно пополняющаяся пленочная жидкая вода за счет подплавления льда. Это обстоятельство имеет очень большое народнохозяйственное значение при строительстве самых разнообразных подземных хранилищ в условиях многолетнемерзлых грунтов.
1.8 Твердая вода.
Когда произносят слово «вода», то подразумевают обычно, что речь идет о жидкости. Но вода часто находится в твердом состоянии — в виде льда.
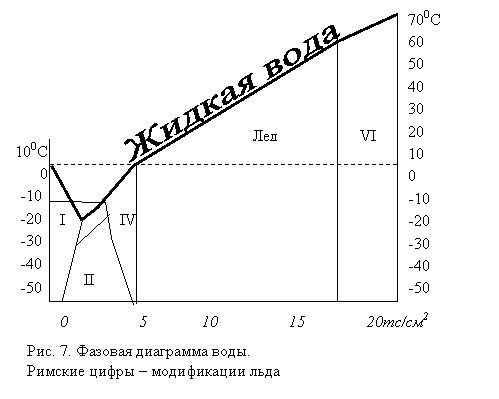
В первой четверти нашего века немецкий химик Г. Тамман и американский физик П. Бриджмен выявили шесть разновидностей льда, различающихся давлениями и температурами (рис. 7):
Лед I - обыкновенный лед, существующий при давлении до 2200 аты, устойчивый в нормальных условиях, при дальнейшем повышении давления (выше 2200 атм) переходит в разновидностьII.
Лед II-с уменьшением объема на 18—20% тонет в воде, его плотность 1,2 г/см3 (при 0°С), очень неустойчив, легко переходит в модификацию III.
Лед III - также тяжелее воды (его плотность больше плотности льда I, из которого непосредственно может быть получена описываемая модификация, на 5%).
Лед IV -легче воды, существует при небольшом давлении и температуре немного ниже О "С, неустойчив и легко переходит в разновидность I.
Лед V — может существовать при давлении от 3,6 до 6,3 кбар, его плотность выше плотности льда III на 5,5 и воды на 6%.
Лед VI -может быть получен непосредственно из воды при температуре 60 °С и давлении 16,5 кбар (при давлении 21 кбар температура этой модификации льда 76 "С), его плотность выше плотности льда V на 4 и воды на 6%.
 |
