Влияние хрома на электрохимическое поведение сталиСтраница 1
1. Пассивность металлов.
Пассивностью металлов называют состояние довольно высокой коррозионной стойкости , вызванное торможением анодного процесса электрохимической коррозии .
Повышенная коррозионная стойкость металлов может обуславливаться:
а) термодинамической устойчивостью металла ;
б) отсутствием в электролите деполяризатора;
в) затруднённостью доставки деполяризатора к поверхности металла;
г) сильным торможением протекания катодного процесса ;
и другими причинами .
|
|
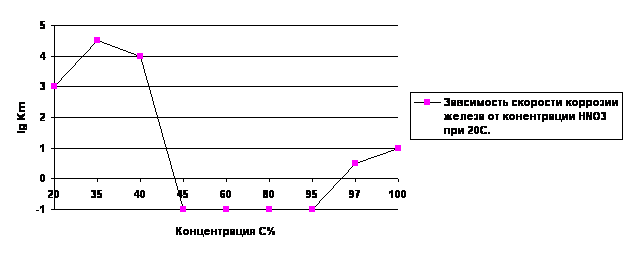
Типичным примером пассивности металлов является резкое уменьшение скорости растворения железа в растворах азотной кислоты, наступающее при достаточно высокой её концентрации .
Пассивность наблюдается в определённых условиях у титана , алюминия , хрома , молибдена , магния и других металлов . Очень многие металлы в той или иной степени в зависимости от условий склонны пассивироваться .
Наступление пассивного состояния металлов характеризуется следующими явлениями:
а) резким уменьшением скорости коррозии металла;
б) значительным смещением потенциала металла в положительную сторону : для железа от значений (-0.2)¸(-0.5)В к значениям +0.5¸(+1.0)В
для хрома - от (-0.4)¸(-0.6)В до +0.9В .
Смещение потенциала указывает на то , что при наступлении пассивности затормаживается протекание анодного процесса электрохимической коррозии . Пассивности металлов обычно соответствует высока степень анодного контроля коррозионного процесса.
Пассиваторами обычно являются :
а) окислители ;
б) анодная поляризация от внешнего источника постоянного электрического тока или при работе металла в качестве анода с другим металлом , являющимся катодом , которая в подходящих условиях при достижении определённого значения эффективного потенциала металла Vме и соответствующей ему анодной плотности тока i(а) может вызвать наступление пассивного состояния металла .

2. Плёночная теория пассивности металлов .
Согласно этой теории пассивное состояние металла обуславливается присутствием на его поверхности окисных плёнок .
Чаще всего эти плёнки представляют собой окислы Fe3O4 или Fe8O11на железе в HNO3 , смешанный окисел Cr2O3 и СrO2 на хроме в кислых средах .
Такая плёнка образуется в качестве превичного нерастворимого продукта анодного процесса на анодных участках , что происходит при потенциалах , более отрицательных, чем потенциал анодной реакции выделения кислорода , и приводит к сильному торможению анодного процесса .
Пассивная плёнка электропроводна и играет роль катода , в то время как анодный процесс протекает в порах плёнки под воздействием очень большой плотности тока , что создаёт условия для образования и перехода в раствор в небольшом количестве ионов металла высшей валентности .
Поры закрываются вследствие образования плёнки окислов и сова возникают в других местах , где имеет место растворение плёнки или её катодное восстановление . Явление пассивности представляет собой динамическое равновесие между силами , создающими защитную плёнку , и силами, нарушающими её сплошность (водородными и галоидными ионами , катодной поляризацией и др.) .
Коррозионная стойкость металла в пассивном состоянии зависит от совершенства образующейся защитной плёнки , количества и размеров её пор , а устойчивость пассивного состояния определяется устойчивостью защитной плёнки в данных условиях.
3. Адсорбционная теория пассивности металлов.
Эта теория предполагает возникновение на металлической поверхности мономолекулярных адсорбированных слоёв кислорода, окислителя и других веществ , сплошь заполняющих поверхность или наиболее активные участки поверхности (углы и рёбра кристаллической решётки и др.) .